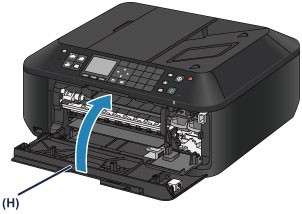
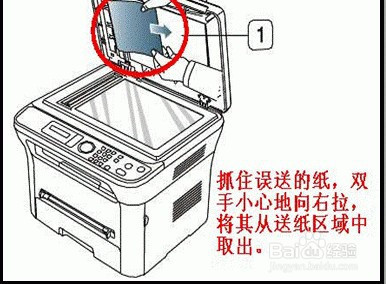
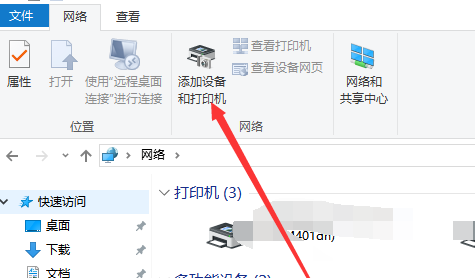
电脑连接打印机怎么扫描(电脑连接打印机怎么扫描成pdf)
回想刚刚入行的两年里,负责的项目先后经历了FDA视察小组、稽查和国家局检查 ,一直在准备被查的路上,比较开心的事情是三个项目均顺利通过了核查,并已经上市,在此过程中也有一点小小的体会,给大家分享一下。
在新版GCP中,检查,指药品监督管理部门对临床试验的有关文件、设施、记录和其他方面进行审核检查的行为,检查可以在试验现场、申办者或者合同研究组织所在地,以及药品监督管理部门认为必要的其他场所进行。
在《总局关于印发药物临床试验数据核查工作程序(暂行)的通知》食药监药化管(2016)34号中 第三条:核查中心应将现场核查计划在其网站公示10个工作日,注明联系方式与反馈时限要求,并告知药品注册申请人,同时告知其所在地省级食品药品监管部门。
在核查公示以后,
我们CRC可以做哪些准备呢?
核查前
1、 与CRA和PM进行沟通,确认项目是否撤回,预计可能的检查时间,通常以下的几种情况抽中的概率较大:
· 组长单位(如有);
· 入组例数多;
· 入组速度快;
· 有PK采血的中心;
· 筛选成功率/失败率高;
· 项目质量可能有问题的中心。
2、 通知机构和伦理和专业组人员,协助机构或项目组制订自查计划,根据药物临床试验数据现场核查要点内容进行。
3、 与CRA沟通,确认CRO公司自查的安排。
4、 提前了解中心的各项流程,如:病历借阅流程、HIS系统查询流程、血样采集流程、影像流程、发药流程等。并与相关人员进行告知,如涉及某些特殊科室,例如信息科,需要由PI提前进行沟通。
5、 物资准备:核查中可能用到的打印机、电脑等设备,提前联系科室相关人员安排接收。
6、 CRC在准备过程中发现问题要及时进行记录与反馈,如果有疑问与研究者进行确认,且不可擅自修改。
7、 熟悉项目中文件夹内容,提前做好应答准备。
核查中
在核查当日,核查组人员会在通知的时间里亲临研究中心。
在核查的启动会议上,核查组人员宣读法规及纪律要求等、机构、伦理、研究团队人员一同到场,通常是由PI通过PPT对方案要点、本中心研究进展情况等进行介绍,然后开始现场核查工作。
核查时间一般是2-3天,之前我参与的是组长单位,会有其他研究中心的核查组人员汇合,进行了4天多的时间。核查组人员一般会进行分工合作,药物管理、ISF文件、原始病历和EDC中的数据核查由专人进行,因当时是肿瘤项目,还有一位核查人员核查了受试者的影像数据。
在核查过程中,核查人员会现场进行提问,也可能会单独约见相关人员进行问答。这个过程中可以针对核查人员的问题予以解释。关于问答有一些要点:
核查后
在最后结束的会议上,核查组人员会宣读核查的问题,研究者对报告上的内容进行确认。CRC需要协助进行文件的清点与核对,协助研究中心相关人员和申办方在规定的时间内(一般一周以内)完成报告的回复意见,原件由PI签字/院方盖章/原件寄送给申办方或者由机构直接寄送国家局。
另外,做好物资回 收工作,将打印机/备用电脑等寄回申办方/CRO公司。
总结
从个人来看,核查会重点关注数据的真实性与受试者的安全性两个大方面,项目中存在问题是很正常的,我们在日常工作过程中,就要从细节做起,保证每一步按照方案和法规的要求进行操作,如实进行记录。
对于患者安全性方面,比如对于患者的AE情况进行及时协助研究者进行跟进,以免发生漏记AE和SAE漏报的情况。也许我们整个临床研究很小的一份子,但只有我们每一人做好自己的职责,保证共同推动行业的发展与进步。
作者简介
新药不能停,多年CRC及人员管理经验,药研社APP社区内容合作官。
更多临研干货内容
可至【药研社APP】学习讨论
临研人学习交流社区
戳“阅读原文”,打开临研圈
版权声明
本文内容均来源于互联网,版权归原作者所有。
如侵犯到您的权益,请及时通知我们,我们会及时处理。